Denna information vänder sig i första hand till forskare. Det är sammandrag av vår forskningsplan på svenska.
Du kan ladda ned den senaste versionen av forskningsplanen här.
Syfte med EFFECTS
Syftet med EFFECTS är att undersöka om behandling med en kapsel fluoxetin 20 mg per dag under 6 månader efter akut stroke förbättrar patientens funktionsförmåga. Vi inkluderar både ischemisk och haemorrhagisk stroke.
Primär uppföljning (Primary outcome)
Det primära utfallsmåttet är andelen oberoende överlevande definierat som modifierad Rankin Scale (mRS) 0-2 vid sex månader.
Sekundära uppföljningar (Secondary outcomes)
- Överlevnad vid 6 och 12 månader
- Påverkan av det dagliga livet mätt med Stroke Impact Scaele
- Livskvalitet mätt med skalan EQ5D-5L
- Påverkan av vitaliet och trötthet mätt med en en subskala av Health Questionnaire
- Förekomst av depression DSM-IV och skalan MADRS
- Kognition, påverkan på minne och koncentration mätt med MoCA
- Neurologisk status inklusive förekomst av påverkan på muskelkraften eller talförmågan mätt med NIHSS
Studietyp
En akademikerdriven prospektiv randomiserad placebo kontrollerad multicenter, trippel blind med parallell grupp.
Patienterna randomiseras dag 2-15 efter stroke till antingen fluoxetin 20 mg en kapsel eller identisk placebo-kapsel per dag under 6 månader. Allokeringen är i förhållandet 1:1.
Inklusionskriterier
- Ålder över 18 år
- Informerat samtycke kan endast ges av patient som enligt prövaren är beslutskapabel och som efter att ha erhållit information och getts möjlighet att få svar på sina frågor, är villig att delta i studien.
- DT av hjärnan förenlig med intracerebral blödning eller ischemisk stroke
- Randomisering 2 till 15 dagar efter strokeinsjuknande
- Bestående och betydande bortfallssymtom, sett ur den behandlade läkarens och patientens eller närståendes perspektiv.
Exklusionskriterier
- Subaraknoidalblödning
- Ej tillgänglig för uppföljning under 12 månader
- Icke-svensk talande och avsaknad av nära anhörig som kan hjälpa till att besvara formulär på svenska
- Livshotande sjukdom som med hög sannolikhet leder till död inom 12 månader
- Anamnes på krampanfall eller allergi mot fluoxetin
- ASAT eller ALAT > 3 gånger över referensnivån
- Njursvikt (S-Kreatinin > 180 mikromol/L)
- Gravid eller ammande kvinna. Kvinna i fertil ålder måste ha ett fullgott preventivmedel under studien (minst oralt antikonceptionsmedel). Graviditetstest (HCG) krävs före inkludering och efter studiens genomförande.
- Tidigare självmordsförsök
- Pågående depression eller depression den senaste månaden som krävt SSRI-behandling
- Pågående behandling som har allvarlig interaktion med SSRI. Samtidig behandling med monoaminooxidas-hämmare (MAOI) kan leda till livshotande interaktioner varför patienter som behandlas med MAOI-läkemedel inte kan inkluderas i studien. Dessutom, om behandling med MAOI är indicerad för en patient inkluderad i studien, krävs 5 veckor utsättande av studieläkemedel innan behandlingen med MAOI kan påbörjas.
- Patienten redan inkluderad i en CTIMP (Clinical Trial of an Investigational Medicinal Product).
Försiktighet föreligger vid samtidigt användande av seritonergt aktiva smärtstillande läkemedel, t.ex. tradolan och medel mot migrän, t.ex. sumatriptaner. Vid inkludering bör man också vara medveten om möjliga interaktioner mellan SSRI och NSAID (non steroidal anti-inflammatory drugs) där samtida bruk ökar risken för blödningar i den övre magtarm-kanalen.
Randomisering
Patienterna randomiseras via en säker internetförbindelse och studiearmarna balanseras genom så kallad minimisering utifrån fyra faktorer:
- Tid efter insjuknande (2-8 vs 9-15 dagar)
- Predicerat utfall vid 6 månader, baserat på sex enkla variabler
- Förekomst av motoriskt bortfall
- Förekomst av dysfasi
Uppföljning för det lokal centret
Enkel uppföljning från lokala center
- Telefonuppföljning (eller uppföljning inneliggande) 1 vecka efter påbörjade av studieläkemedel ( +/- 3 dagar). Biverkan, tar patienten alla läkemedel, tar 5-10 minuter.
- Telefonuppföljning vid 1 månad (+/- 7 dagar). Samma som 1 vecka, tar 5-10 minuter.
- Kort återbesök vid 3 månader (+/- 7 dagar) till lokalt center för att erhålla läkemedel. Kontroll av biverkningar, man får läkemedel för resterande period 3 månader. Besöket tar cirka 30 minuter. Kan utföras av sjuksköterska eller läkare.
- Vid 6 månader (+/- 14 dagar) sker återbesök till lokalt center. Tar cirka 1 timme. Kan utföras av sjuksköterska eller läkare.
- Telefonuppföljning vid 7 månad (+/- 7 dagar). Samma som 1 vecka, tar 5-10 minuter.
Uppföljning centralt
- Vid 6 månader, modifierad Rankin Scale
- Vid 12 månader, modifierad Rankin Scale samt enkät
Statistiks beräkning
EFFECTS siktar på att inkludera 1 500 patienter i Sverige vid ett 25-tal centra. Vid 1 450 patienter fås 90 procent power (vid α=0.05) att upptäcka en 7,5 % absolut ökning av andelen mRS 0-2, från 27,0 % till 34,5 %. Dessutom planerar vi att poola våra data med två andra studier, FOCUS-UK (Storbritannien) och AFFINITY (Australien) vilka trots att varje studie har egen statistisk power for huvudeffektvariabeln och egen design ändå har gemensamt upplägg och utfallsmått.
Det finns flera fördelar med att genomföra tre separata studier med gemensamt studieupplägg. Antalet patienter ökar. Tillsammans beräknas vi kunna inkludera 6 000 patienter, vilket möjliggör kliniskt relevanta subgruppsanalyser. Vi uppnår samordningsvinster genom att vi kan använda samma farmaka- och placebotillverkare samt likadana, men oberoende, randomiserings-system.
Ordförandena i våra respektive data och säkerhetskommittéer kan samordna tolkningsfrågor och bedömningar. Samtidigt kommer vi att kunna fastställa den externa validiteten (generaliserbarheten) genom de tre separata studierna med samma kärndesign.
2014: startfas
Studien kommer att drivas i två direkt på varandra följande faser, startfas och huvudfas.
Startfasen inleddes hösten 2014 och 50 patienter vid Danderyds sjukhus samt Karolinska Universitetssjukhuset (Solna) samt Enköpings lasarett inkluderas. Syftet är att etablera det team som leder studien, undersöka rekryteringstakten och testa logistiken inklusive uppföljningsformulär och complience.
Studieprotokollet kommer att bli föremål för ändringar. Den oberoende data- och säkerhetskommittén gör årligen en till två avblindade bedömning av studien och ska råda EFFECTS styrkommitté.
2015 – 2016: huvudfasen
Under huvudfasen expanderar studien till cirka 35 center i Sverige. Varje center förväntas bidra med 24 patienter per år. Patientens ansvarige läkare och sjuksköterska finns på det lokala centret där baslinje undersökningar görs och dit patienten vänder sig med frågor.
EFFECTS omfattar lokal undersökning av motorfunktion, kommunikation, och kognition vid baslinjen och 6 månader. Depression undersöks enligt DSM-IV intervju per telefon eller återbesök vid 1 vecka, 1 månad och vid 7 månader.
Under behandling följs sidoeffekter av ansvarig sköterska på lokalt centret i samråd med ansvarig läkare. Uppföljningar av huvudeffektvariabel och patientskattningar på 6- och 12- månaders nivå görs därtill centralt med frågeformulär eller per telefon från koordinerande center för säker blindning.
Huvudeffektvariabel är mRS, och patienten skattar också själv sin funktion i Stroke Impact Scale; sin emotionella situation, och vitalitet på två subskalor till Hälsoenkät: och den hälso-relaterade livskvaliteten enligt EuroQual.
Study assessment scedule
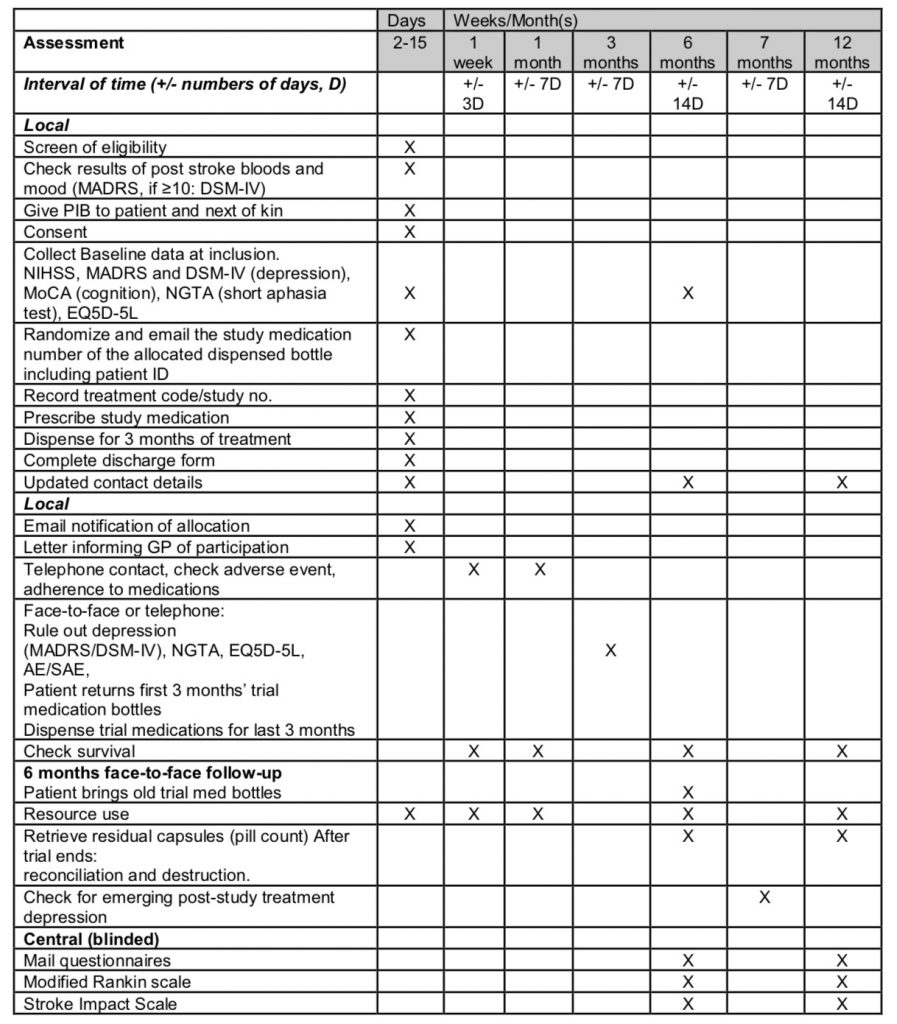
Bilden nedan visar också en översikt av inkludering och uppföljning av studien.
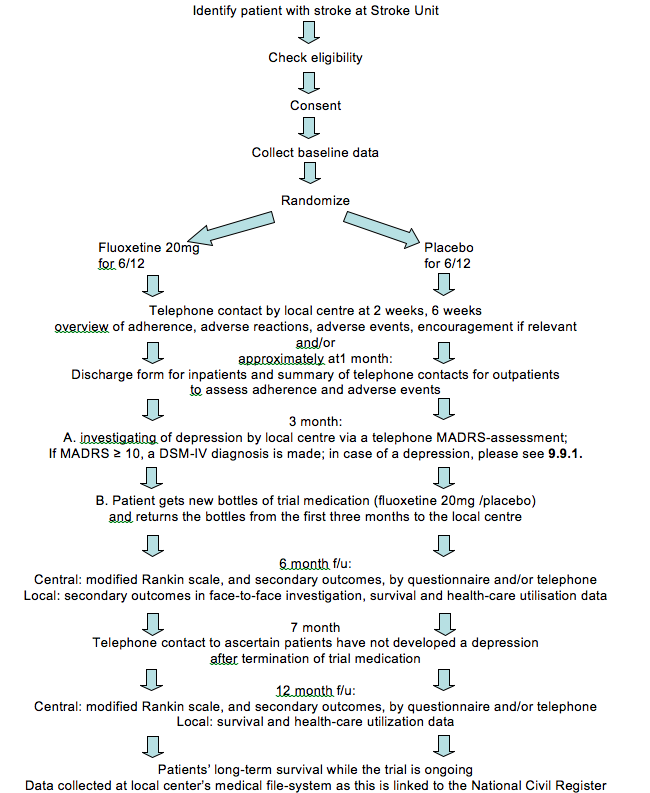
2017 – 2019: avslutningsfas
Avslutning av studien. Huvudfynd publiceras. Samarbete inom ramen för EFFECTS, FOCUS och AFFINITY fortsätter med externa validitets-data. Publiceras i tidskrift samt inom the Cochrane Collaboration.